新加坡市场是医疗器械出口商的一片沃土,而理解和遵循其法规和制度是获得成功的关键。这篇文章将深入剖析新加坡的医疗器械行业的立法背景、产品定义和分类,以及市场准入过程。
新加坡的医疗器械行业遵循一套详细而严格的法规和指导方针。直至2007年,对大多数医疗器械的注册是自愿的,尽管制造商或其当地代理商仍需要确保产品符合安全、质量和性能的各项要求。但对于高风险医疗器械,其在新加坡卫生科学局的注册是必要的。参考了各个发达国家的医疗器械监管系统后,新加坡在2007年制定了《健康产品法令》并发布了一系列的指导文件,从而形成了一套适合自身的医疗器械监管体系。新加坡卫生科学局(HSA)作为卫生部下属的法定管理机构,具体负责医疗器械的监管工作。
在新加坡,医疗器械被定义为单独或组合使用,目的在于诊断、预防、监测、治疗或减轻疾病,或者是支持或维持生命等用途的产品。医疗器械按风险程度被分为四个等级,从A级(低风险)到D级(高风险)。
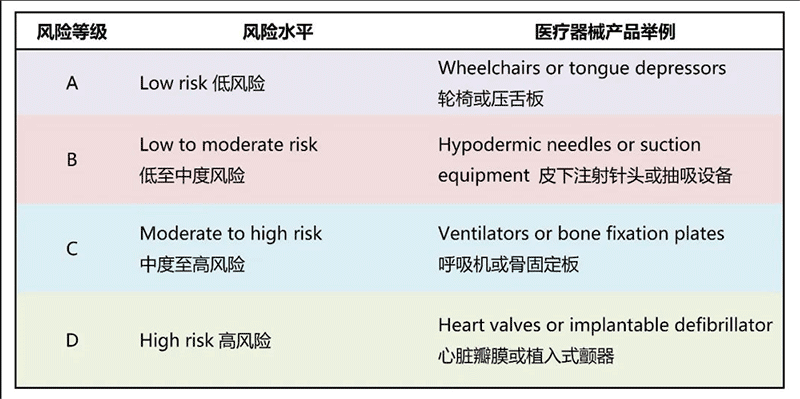
进入新加坡医疗器械市场,首先需要满足新加坡卫生科学局的严格要求。从2007年开始,HSA不断加强对医疗器械的监管力度,并逐步实施相应的监管策略。所有类别的医疗器械产品(除非被豁免)都必须经过HAS注册后才能在新加坡上市销售。注册人或申请人必须是在新加坡注册的公司,并需要确保其医疗器械列入新加坡医疗器械注册清单中。
然而,对于在美国、欧盟、澳大利亚、日本获得批准,或有安全使用历史的医疗器械,新加坡可能会采用简化、加速和即时的评估方式。根据设备的风险等级,注册一款产品通常需要3至12个月的时间。
另外,新加坡对于代表制度也有明确的规定。制造商如果在新加坡有当地主体,则可以直接在HSA网站上完成注册。若无,必须指定当地代表进行申请。医疗器械的注册人不仅需要提交注册申请,还需要负责上市后的活动,包括警惕性报告、修改申请等。
最后,新加坡也有一套明确的医疗器械审核流程。对于未经HSA任何海外参考监管机构事先批准的医疗器械,必须经过全面评估。而所有企业在新加坡制造、进口或供应医疗器械之前,都必须获得经销商许可证。
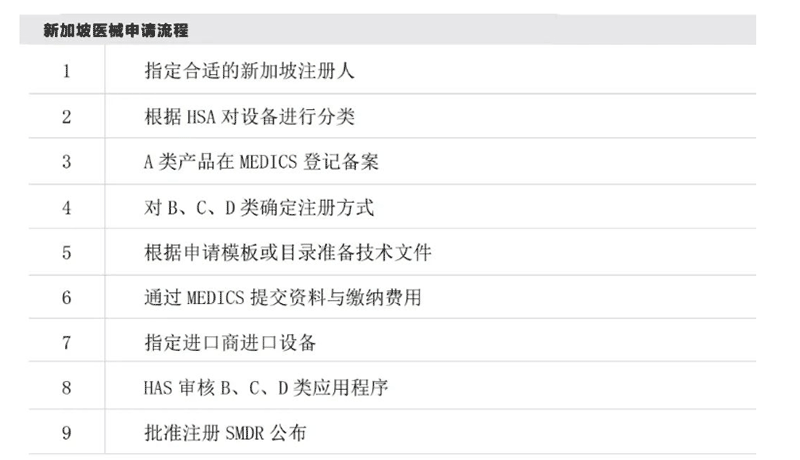
总的来说,进军新加坡市场,需深入了解并严格遵循当地的法规,以确保医疗器械产品的安全、质量和效果,同时也为企业赢得市场份额,实现持续发展。




 在线问专家
在线问专家

